Quel rôle jouent les dérivés de la pyrimidine dans les systèmes biologiques ?
Nov 07,2025Comment les dérivés de triazine agissent-ils comme agents antimicrobiens ou antifongiques ?
Oct 24,2025Qu’est-ce qui rend les dérivés du carbazole chimiquement stables ?
Oct 17,2025Comment les dérivés du carbazole se comportent-ils dans des conditions acides ou basiques
Oct 10,2025Les dérivés du furane peuvent-ils être préparés à partir de biomasse renouvelable ?
Oct 03,2025Dérivés de pyrimidine , célébré pour leur polyvalence et leur omniprésence en chimie organique, servent de pinnes dans de nombreuses transformations chimiques. Parmi ceux-ci, les réactions de substitution nucléophile se distinguent comme une pierre angulaire des méthodologies synthétiques. Ces réactions soulignent non seulement la réactivité des pyrimidines, mais débloquent également les voies des architectures moléculaires complexes.
Les subtilités de la substitution nucléophile
Les réactions de substitution nucléophile impliquant des dérivés de pyrimidine sont régies par la nature déficiente en électrons inhérente du cadre hétérocyclique. Les atomes d'azote incrustés dans le système d'anneaux créent des régions d'électrophilicité, rendant des positions spécifiques, telles que C2, C4 et C6 - capables d'attaquer par des nucléophiles. Cette sensibilité est encore accentuée par la présence de groupes activateurs ou laissant des fonctionnalités attachées au noyau de pyrimidine.
Voies de réaction clés
Mécanisme SNAR: substitution nucléophile aromatique
Le mécanisme de substitution nucléophile aromatique bimoléculaire (SNAR) est peut-être la voie la plus emblématique de ce domaine. Ici, un groupe d'électrons, comme un substituant nitro ou cyano, active l'anneau de pyrimidine vers l'assaut nucléophile. Le processus se déroule à travers la formation d'un complexe fugace de Meisenheimer - un intermédiaire stabilisé par résonance - se terminant avant l'expulsion du groupe de départ. Ce mécanisme trouve une application approfondie dans la synthèse pharmaceutique, en particulier dans la création d'échafaudages bioactifs.
Mécanisme SN2: substitution aliphatique aux sites exocycliques
Lorsque les dérivés de pyrimidine portent des groupes fonctionnels exocycliques, tels que des halogénures ou des sulfonates, ils se prêtent à des substitutions de type SN2. Ces réactions se déroulent avec l'inversion de la configuration au centre réactif, offrant un contrôle précis sur les résultats stéréochimiques. Ces transformations sont indispensables dans l'assemblage des intermédiaires chiraux et des analogues de produits naturels.
Réactions de couplage transversal catalysées en métal
La catalyse des métaux de transition a révolutionné le paysage des substitutions nucléophiles. Les couplage croisé catalysé par le palladium ou le nickel permettent l'introduction de divers nucléophiles - en passant par les réactifs organométalliques aux acides boroniques - dans des sites spécifiques sur l'échafaudage de pyrimidine. Cette approche transcende les limitations traditionnelles, offrant un accès à un vaste répertoire de dérivés substitués.
Séquences d'élimination promotionnelle de base
Dans des conditions de base, les dérivés de pyrimidine peuvent subir des séquences d'élimination-addition. Ces processus impliquent souvent le départ initial d'un groupe de départ, suivi de l'interception de l'électrophile résultante par un nucléophile. Ces réactions en tandem sont particulièrement avantageuses lors de la construction de systèmes densément fonctionnalisés.
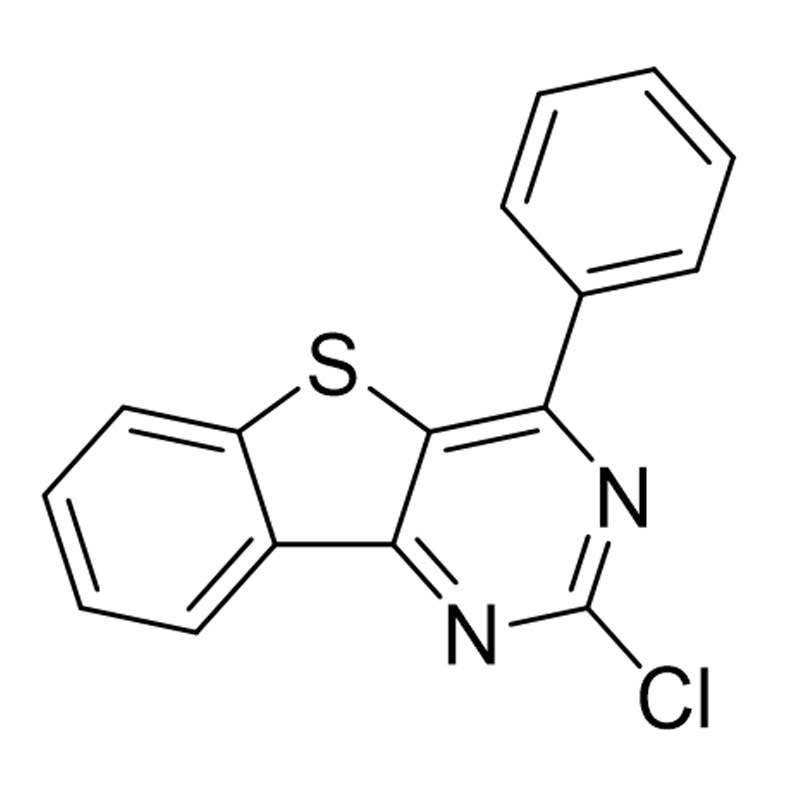
Facteurs influençant la réactivité
L'efficacité des réactions de substitution nucléophile dépend de plusieurs facteurs. La modulation électronique du noyau de pyrimidine - a été consacrée à la mise en place judicieuse des substituants - peut améliorer ou atténuer la réactivité. L'obstruction stérique, la polarité du solvant et la température dictent encore le cours de ces transformations. La maîtrise de ces variables permet aux chimistes d'adapter les conditions de réaction aux résultats souhaités.
Applications entre les disciplines
L'attrait des substitutions nucléophiles à base de pyrimidine s'étend bien au-delà de la curiosité académique. En chimie médicinale, ces réactions facilitent la synthèse des inhibiteurs de la kinase, des agents antiviraux et des thérapies anticancéreuses. Les applications industrielles abondent également, avec des dérivés de pyrimidine mettant en évidence les formulations agrochimiques et les innovations scientifiques des matériaux.
Les réactions de substitution nucléophile impliquant des dérivés de pyrimidine incarnent la confluence de l'élégance et de l'utilité dans la synthèse organique. En tirant parti des attributs électroniques et structurels uniques des pyrimidines, les chimistes continuent de repousser les limites de la conception moléculaire. Que ce soit dans le laboratoire ou sur le plancher de production, ces réactions restent un atout inestimable dans la poursuite de nouveaux composés et des découvertes révolutionnaires.

